NRicher™ C
货号:NRCO-10
品牌:Biotech Support Group
产品特性
用于补体级联相关蛋白的富集
可从动物或人血清/血浆或细胞裂解液中富集补体级联相关蛋白
非抗体来源,具有物种普适性
Bead格式兼容自动化系统
| 规格 | 价格 |
|---|---|
| 10 preps | ¥咨询 |
产品咨询:info@biopcr.com
产品订购:sales@biopcr.com
技术支持:tech@biopcr.com
服务热线:400-860-6200
详细介绍
产品名称:NRicher™ C
别名:NRicher C - Enrichment of Complement Cascade Related Proteins;NRicher C补体级联相关蛋白富集试剂
NRicher™ C
补体级联相关蛋白富集试剂
• 采用化学衍生珠耗材,由于非抗体来源,具有物种普适性,不限制物种
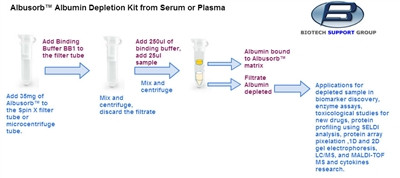
• 可从动物或人血清/血浆或细胞裂解液中富集补体级联相关蛋白,白蛋白去除率>90%
• 无需特殊仪器,仅需常规微量离心机即可
• Bead格式兼容自动化系统
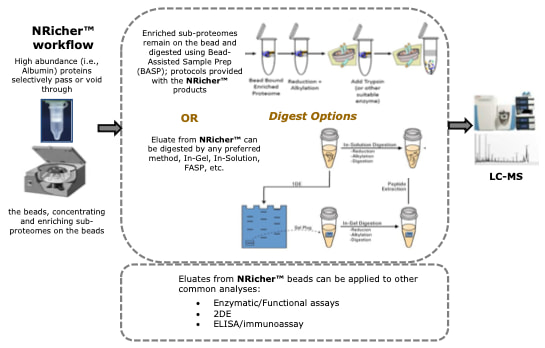
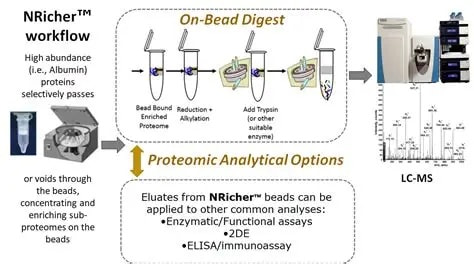
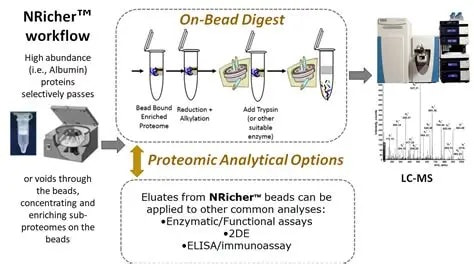
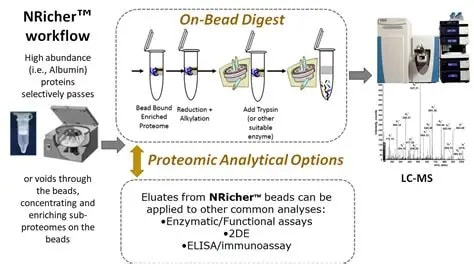
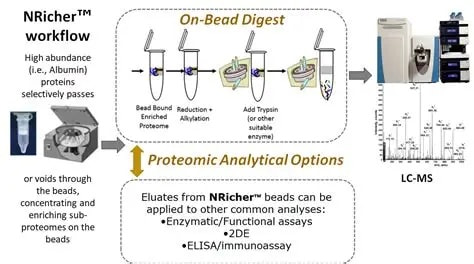
• 支持珠上酶解以用于LC-MS分析,也可选择洗脱后进行其他酶解,或用于其他功能分析,酶活或免疫分析
补体级联是免疫系统的重要组成部分,提供强大的宿主监视功能,保护机体免受入侵微生物侵害。它还能与抗体协同作用,促进B细胞和T细胞活化,从而对适应性免疫应答产生重要影响。细胞内活性补体系统——Complosome,已被证明在调节T细胞反应、细胞生理学(如代谢)以及炎性疾病进程中发挥着关键作用。补体失调与多种慢性疾病相关,例如年龄相关性黄斑变性、阵发性睡眠性血红蛋白尿症(PNH),以及神经、心血管和肿瘤疾病。在急性炎症状态下,过度活跃的补体可能导致个体不良预后,这在住院的Covid-19患者中已被观察到。
补体系统由50多种循环蛋白和膜蛋白组成,约占血浆总蛋白质量的5%。大多数补体蛋白以无活性前体(酶原)形式在血液中循环,一旦被触发,便会通过蛋白水解级联反应被激活。尽管教科书描述了三条激活途径(经典途径、凝集素途径和旁路途径)最终形成C3转化酶蛋白复合物,但补体系统还与凝血系统相互关联,以清除受损组织、激活血小板并在损伤时促进止血。反之,补体也可直接被凝血过程衍生的蛋白水解酶激活(凝血酶、激肽释放酶)。补体激活会产生多种效应,包括:调理病原体或受损的自身细胞以增强吞噬作用;产生过敏毒素C3a和C5a;募集白细胞至炎症部位;以及级联反应的终末环节——在细胞表面组装膜攻击复合物(MAC)。
补体级联的终末端来源于C3转化酶的蛋白水解产物——C5b,它依次募集C6、C7、C8和C9,组装成膜攻击复合物(MAC)。该复合物也被称为“末端补体复合物”,其形成始于C5b-7插入细胞膜,随后捕获C8并诱导C9环状聚合——每个孔道可聚合多达18个C9分子。终末膜攻击复合物会在入侵病原体或靶细胞的细胞膜上穿孔,当足够数量的膜攻击复合物(MAC)孔形成时,细胞会因渗透性裂解而死亡。然而,亚致死剂量的MAC所产生的效应与致死剂量显著不同,包括促进细胞黏附、聚集、趋化、细胞分裂以及细胞外囊泡的释放。
在这一关键环节中,补体系统必须在激活与抑制之间保持精妙的平衡,以便在必要时激活以对抗感染因子或修饰的自身/宿主组织,同时保护健康的自身/宿主组织。这种保护作用通过调节蛋白和抑制因子的协同作用系统性实现,从而确保对正常健康至关重要的细胞和组织的完整性。尽管补体系统在疾病和健康中如此重要,但目前可用于临床实践的生物标志物却十分有限:目前主要采用总C3和C4免疫测定,并在怀疑缺陷时测定补体活性(CH50溶血测定)。蛋白质组学研究有望为急慢性疾病发现新的补体生物标志物。
返回列表
补体级联相关蛋白富集试剂
• 采用化学衍生珠耗材,由于非抗体来源,具有物种普适性,不限制物种
• 可从动物或人血清/血浆或细胞裂解液中富集补体级联相关蛋白,白蛋白去除率>90%
• 无需特殊仪器,仅需常规微量离心机即可
• Bead格式兼容自动化系统
• 支持珠上酶解以用于LC-MS分析,也可选择洗脱后进行其他酶解,或用于其他功能分析,酶活或免疫分析
补体级联是免疫系统的重要组成部分,提供强大的宿主监视功能,保护机体免受入侵微生物侵害。它还能与抗体协同作用,促进B细胞和T细胞活化,从而对适应性免疫应答产生重要影响。细胞内活性补体系统——Complosome,已被证明在调节T细胞反应、细胞生理学(如代谢)以及炎性疾病进程中发挥着关键作用。补体失调与多种慢性疾病相关,例如年龄相关性黄斑变性、阵发性睡眠性血红蛋白尿症(PNH),以及神经、心血管和肿瘤疾病。在急性炎症状态下,过度活跃的补体可能导致个体不良预后,这在住院的Covid-19患者中已被观察到。
补体系统由50多种循环蛋白和膜蛋白组成,约占血浆总蛋白质量的5%。大多数补体蛋白以无活性前体(酶原)形式在血液中循环,一旦被触发,便会通过蛋白水解级联反应被激活。尽管教科书描述了三条激活途径(经典途径、凝集素途径和旁路途径)最终形成C3转化酶蛋白复合物,但补体系统还与凝血系统相互关联,以清除受损组织、激活血小板并在损伤时促进止血。反之,补体也可直接被凝血过程衍生的蛋白水解酶激活(凝血酶、激肽释放酶)。补体激活会产生多种效应,包括:调理病原体或受损的自身细胞以增强吞噬作用;产生过敏毒素C3a和C5a;募集白细胞至炎症部位;以及级联反应的终末环节——在细胞表面组装膜攻击复合物(MAC)。
补体级联的终末端来源于C3转化酶的蛋白水解产物——C5b,它依次募集C6、C7、C8和C9,组装成膜攻击复合物(MAC)。该复合物也被称为“末端补体复合物”,其形成始于C5b-7插入细胞膜,随后捕获C8并诱导C9环状聚合——每个孔道可聚合多达18个C9分子。终末膜攻击复合物会在入侵病原体或靶细胞的细胞膜上穿孔,当足够数量的膜攻击复合物(MAC)孔形成时,细胞会因渗透性裂解而死亡。然而,亚致死剂量的MAC所产生的效应与致死剂量显著不同,包括促进细胞黏附、聚集、趋化、细胞分裂以及细胞外囊泡的释放。
在这一关键环节中,补体系统必须在激活与抑制之间保持精妙的平衡,以便在必要时激活以对抗感染因子或修饰的自身/宿主组织,同时保护健康的自身/宿主组织。这种保护作用通过调节蛋白和抑制因子的协同作用系统性实现,从而确保对正常健康至关重要的细胞和组织的完整性。尽管补体系统在疾病和健康中如此重要,但目前可用于临床实践的生物标志物却十分有限:目前主要采用总C3和C4免疫测定,并在怀疑缺陷时测定补体活性(CH50溶血测定)。蛋白质组学研究有望为急慢性疾病发现新的补体生物标志物。